Kwas pirogronowy to bez wątpienia jeden z najważniejszych związków organicznych, stanowiący pomost między chemią a biologią na poziomie komórkowym. W tym artykule przyjrzymy się dokładnie jego wzorom chemicznym, unikalnej budowie oraz właściwościom, które determinują jego kluczową rolę w metabolizmie. Moim celem jest dostarczenie Wam precyzyjnej wiedzy, która ułatwi zrozumienie, dlaczego ta niepozorna cząsteczka jest tak fascynująca dla chemików i biochemików.
Kwas pirogronowy: kluczowy α-ketokwas o wzorze C₃H₄O₃ w centrum metabolizmu
- Wzór sumaryczny kwasu pirogronowego to C₃H₄O₃, a półstrukturalny CH₃COCOOH.
- Jest najprostszym α-ketokwasem, zawierającym grupę karboksylową (-COOH) i ketonową (C=O).
- Odgrywa centralną rolę w metabolizmie komórkowym, będąc produktem glikolizy i prekursorem cyklu Krebsa.
- W warunkach beztlenowych ulega fermentacji, np. do kwasu mlekowego.
- Posiada masę molową 88,06 g/mol i jest dobrze rozpuszczalny w wodzie i etanolu.
- Znajduje zastosowanie w kosmetologii jako składnik peelingów chemicznych.
Trzy wzory kwasu pirogronowego – który jest najważniejszy?
W chemii organicznej, aby w pełni opisać cząsteczkę, często posługujemy się różnymi typami wzorów. Każdy z nich pełni inną funkcję i dostarcza nam odmiennych informacji. W przypadku kwasu pirogronowego, zrozumienie różnic między wzorem sumarycznym, półstrukturalnym a strukturalnym jest kluczem do pojęcia jego chemicznej natury. Wybór "najważniejszego" zależy tak naprawdę od tego, czego w danej chwili chcemy się o tym związku dowiedzieć. Pozwólcie, że przybliżę Wam każdy z nich.
Wzór sumaryczny C₃H₄O₃: Pierwszy rzut oka na skład
Wzór sumaryczny kwasu pirogronowego to C₃H₄O₃. Jest to najbardziej podstawowy zapis, który informuje nas wyłącznie o składzie ilościowym i jakościowym cząsteczki. Mówi nam, że jedna cząsteczka tego kwasu składa się z trzech atomów węgla, czterech atomów wodoru i trzech atomów tlenu. Chociaż jest to informacja niezbędna, na przykład do obliczeń stechiometrycznych, wzór ten nie mówi nam absolutnie nic o tym, jak te atomy są ze sobą połączone, ani jakie grupy funkcyjne tworzą. Jest to więc jedynie wstęp do poznania struktury związku.
Wzór półstrukturalny CH₃COCOOH: Jak odczytać budowę cząsteczki?
Zdecydowanie częściej w praktyce chemicznej spotkacie się ze wzorem półstrukturalnym (grupowym), który dla kwasu pirogronowego przyjmuje postać CH₃COCOOH. Ten zapis jest znacznie bardziej informatywny. Pokazuje nam sekwencję atomów węgla w łańcuchu oraz, co kluczowe, wyraźnie wyodrębnia obecne w cząsteczce grupy funkcyjne. Odczytując go od lewej, widzimy grupę metylową (CH₃-), połączoną z grupą karbonylową (>C=O, tutaj zapisaną jako CO), która z kolei łączy się z grupą karboksylową (-COOH). To właśnie ten wzór pozwala nam szybko zidentyfikować kwas pirogronowy jako kwas karboksylowy zawierający dodatkowo grupę ketonową.
Wzór strukturalny: Graficzna reprezentacja atomów i wiązań
Najbardziej szczegółowym sposobem przedstawienia jest wzór strukturalny. Jest to pełna graficzna reprezentacja cząsteczki, pokazująca wszystkie atomy oraz każde wiązanie chemiczne (pojedyncze i podwójne) między nimi. Dopiero ten wzór pozwala nam w pełni zrozumieć geometrię cząsteczki, rozmieszczenie przestrzenne grup funkcyjnych oraz hybrydyzację atomów węgla. Choć jego rysowanie jest najbardziej czasochłonne, jest on nieodzowny, gdy analizujemy mechanizmy reakcji chemicznych lub chcemy precyzyjnie wyjaśnić, dlaczego dany związek reaguje w określony sposób. To właśnie na podstawie wzoru strukturalnego chemicy "widzą" przestrzeń reakcyjną cząsteczki.
Zrozumienie tych trzech sposobów zapisu pozwala nam przejść do głębszej analizy tego, co tak naprawdę definiuje ten związek.
Kluczowe elementy budowy – co definiuje kwas pirogronowy?
Unikalne właściwości chemiczne i biologiczne kwasu pirogronowego nie biorą się znikąd. Są one bezpośrednim następstwem obecności dwóch konkretnych grup funkcyjnych w jego niewielkiej cząsteczce. To właśnie ta specyficzna kombinacja sprawia, że kwas pirogronowy jest tak reaktywny i odgrywa tak istotną rolę w naturze. Przyjrzyjmy się im bliżej.
Grupa karboksylowa (-COOH): Skąd biorą się właściwości kwasowe?
Pierwszą i fundamentalną grupą jest grupa karboksylowa (-COOH), zlokalizowana przy pierwszym atomie węgla. To ona decyduje o tym, że omawiany związek jest kwasem organicznym. Grupa ta ma zdolność do donacji protonu (jonu H⁺), co nadaje kwasowi pirogronowemu jego kwaśny charakter. Warto jednak pamiętać, że w warunkach fizjologicznych, czyli wewnątrz naszych komórek, gdzie pH jest bliskie neutralnemu, kwas pirogronowy niemal w całości występuje w postaci zjonizowanej jako anion pirogronianowy (CH₃COCOO⁻). To właśnie pirogronian, a nie kwas w formie niezdysocjowanej, jest głównym aktorem metabolicznych przemian.
Grupa ketonowa (C=O): Dlaczego jest to α-ketokwas?
Drugim kluczowym elementem budowy jest grupa karbonylowa o charakterze ketonowym (>C=O), która znajduje się przy drugim atomie węgla. W nomenklaturze chemicznej węgiel sąsiadujący bezpośrednio z grupą karboksylową oznacza się grecką literą α (alfa). Ponieważ grupa ketonowa znajduje się właśnie w tej pozycji, kwas pirogronowy klasyfikowany jest jako α-ketokwas. Co więcej, ze względu na obecność tylko trzech atomów węgla w łańcuchu, jest on najprostszym możliwym przedstawicielem tej niezwykle ważnej grupy związków. Obecność tej grupy ketonowej w bezpośrednim sąsiedztwie grupy karboksylowej drastycznie wpływa na reaktywność całego związku.
Tautomeria keto-enolowa: Ukryta, mniej stabilna forma kwasu pirogronowego
Mówiąc o budowie kwasu pirogronowego, nie sposób nie wspomnieć o zjawisku tautomerii keto-enolowej. Ze względu na obecność grupy ketonowej i atomów wodoru przy sąsiednim atomie węgla (grupa metylowa), kwas pirogronowy istnieje w równowadze dynamicznej między dwiema formami: dominującą formą ketonową (CH₃COCOOH) a śladową formą enolową (CH₂=C(OH)COOH). Choć forma enolowa jest znacznie mniej stabilna i występuje w znikomych ilościach, możliwość jej powstawania jest kluczowa dla zrozumienia niektórych specyficznych reakcji chemicznych i enzymatycznych, w których bierze udział ten związek. To kolejny dowód na to, jak fascynująca i dynamiczna może być struktura chemiczna.
Teraz, gdy znamy już budowę cząsteczki, możemy łatwo wyjaśnić jej właściwości fizyczne i chemiczne.
Jak wzór wpływa na właściwości fizykochemiczne?
Budowa chemiczna, którą właśnie przeanalizowaliśmy, bezpośrednio przekłada się na mierzalne właściwości fizykochemiczne kwasu pirogronowego. To, jak ta cząsteczka wygląda "na papierze", determinuje to, jak zachowuje się ona w probówce czy w organizmie. Przyjrzyjmy się kilku kluczowym aspektom.
Masa molowa 88,06 g/mol i jej praktyczne znaczenie
Na podstawie wzoru sumarycznego C₃H₄O₃ możemy precyzyjnie obliczyć masę molową kwasu pirogronowego, która wynosi 88,06 g/mol. Dla chemika jest to informacja o fundamentalnym znaczeniu praktycznym. Pozwala ona na przeliczanie masy substancji na liczbę moli i odwrotnie, co jest niezbędne do przygotowywania roztworów o określonym stężeniu oraz do wykonywania wszelkich obliczeń stechiometrycznych związanych z reakcjami, w których kwas pirogronowy bierze udział. Bez tej wartości praca laboratoryjna z tym związkiem byłaby niemożliwa.
Rozpuszczalność w wodzie: Rola grup funkcyjnych
Kwas pirogronowy jest cieczą, która bardzo dobrze rozpuszcza się w wodzie oraz w etanolu. Jak to wyjaśnić na podstawie jego budowy? Kluczem jest obecność dwóch silnie polarnych grup funkcyjnych: karboksylowej i ketonowej. Obie te grupy zawierają atomy tlenu o wysokiej elektroujemności, co pozwala cząsteczkom kwasu pirogronowego na tworzenie silnych wiązań wodorowych z cząsteczkami wody. Ta wysoka polarność i zdolność do interakcji z rozpuszczalnikami polarnymi warunkuje jego doskonałą rozpuszczalność, co ma kluczowe znaczenie dla jego mobilności w środowisku wodnym komórki.
Reaktywność chemiczna: Jakie przemiany umożliwia jego struktura?
Struktura α-ketokwasu czyni kwas pirogronowy związkiem niezwykle reaktywnym chemicznie. Obecność grupy karboksylowej umożliwia typowe dla kwasów reakcje, takie jak tworzenie soli czy estryfikacja. Z kolei grupa ketonowa otwiera drogę do reakcji addycji nukleofilowej czy redukcji. Najbardziej charakterystyczną cechą α-ketokwasów jest jednak ich podatność na reakcje oksydacyjnej dekarboksylacji, czyli jednoczesnego utlenienia i usunięcia grupy karboksylowej w postaci dwutlenku węgla. Ta niezwykła reaktywność, wynikająca bezpośrednio z unikalnego układu grup funkcyjnych we wzorze strukturalnym, jest podstawą jego centralnej roli w metabolizmie.
To właśnie ta chemiczna wszechstronność sprawia, że kwas pirogronowy jest tak ważny dla życia.
Kwas pirogronowy w centrum metabolizmu – dlaczego jest tak ważny?
Wszystko, o czym do tej pory powiedzieliśmy wzory, grupy funkcyjne, właściwości znajduje swoje odzwierciedlenie w biologii. W biochemii kwas pirogronowy (w postaci pirogronianu) nie jest po prostu kolejnym związkiem. Jest to absolutnie kluczowy metabolit pośredni, stanowiący centralny punkt, w którym krzyżują się najważniejsze szlaki energetyczne komórki. Można go przyrównać do głównego dworca kolejowego w metabolicznej mapie organizmu.
Końcowy produkt glikolizy: Jak powstaje z glukozy?
Rola pirogronianu zaczyna się w cytoplazmie, gdzie jest on głównym produktem końcowym glikolizy podstawowego szlaku rozkładu glukozy. W procesie tym jedna cząsteczka glukozy (zawierająca 6 atomów węgla) zostaje, w wyniku serii enzymatycznych reakcji, rozszczepiona na dwie cząsteczki pirogronianu (każda po 3 atomy węgla). Glikoliza dostarcza komórce niewielką ilość energii w postaci ATP, ale jej głównym zadaniem jest właśnie wytworzenie pirogronianu, który jest paliwem do dalszych, znacznie bardziej wydajnych energetycznie etapów.
Na metabolicznym rozdrożu: Dalsze losy pirogronianu w komórce
To, co stanie się z pirogronianem wytworzonym w glikolizie, zależy od warunków panujących w komórce, a przede wszystkim od dostępności tlenu. Pirogronian znajduje się w tym momencie na metabolicznym rozdrożu i to od dostępności tlenu zależy, którą drogę wybierze. Jest on punktem wyjścia dla różnych szlaków. Warto również dodać, że pirogronian jest kluczowym substratem w procesie glukoneogenezy, czyli syntezy glukozy de novo z prekursorów niecukrowych, co pozwala organizmowi utrzymywać odpowiedni poziom cukru we krwi w okresach głodu.
Brama do cyklu Krebsa: Jak pirogronian staje się paliwem dla mitochondriów?
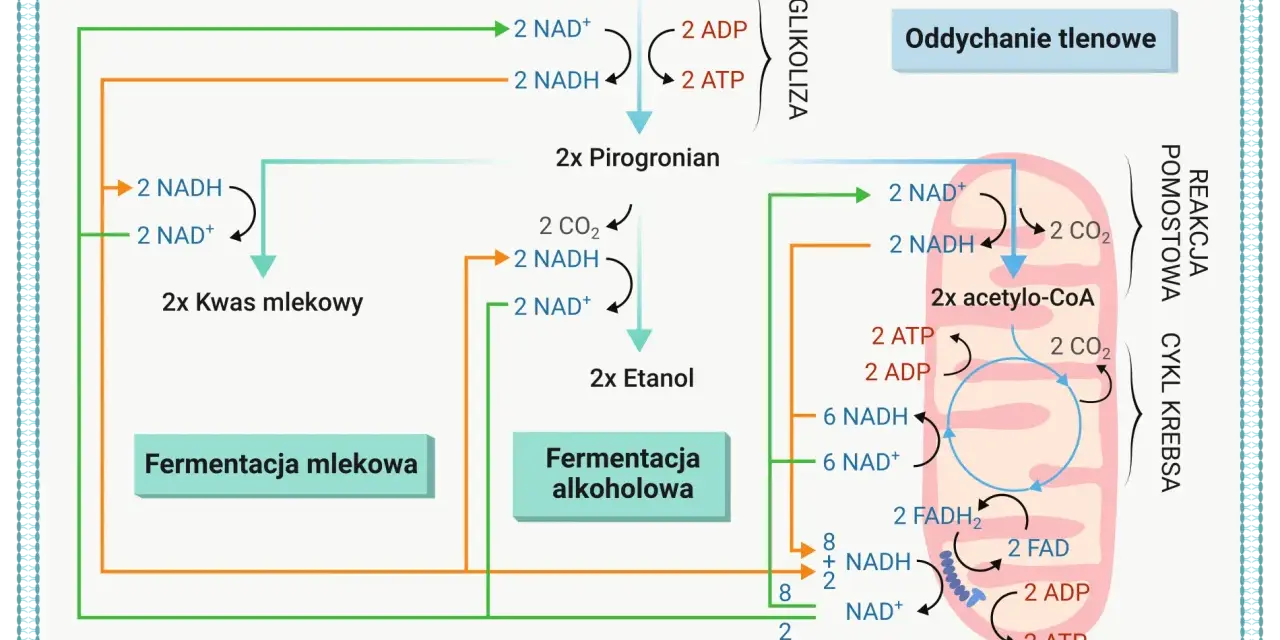
W warunkach tlenowych (aerobowych), pirogronian jest transportowany z cytoplazmy do wnętrza mitochondriów. Tam ulega wspomnianej wcześniej reakcji oksydacyjnej dekarboksylacji, przekształcając się w acetylo-CoA. Ten dwuwęglowy związek jest "aktywnym octanem", który następnie wchodzi do cyklu Krebsa (cyklu kwasu cytrynowego). Cykl Krebsa to centralny szlak utleniania paliw metabolicznych, który dostarcza ogromnych ilości równoważników redukcyjnych dla łańcucha oddechowego, gdzie następuje główna produkcja ATP uniwersalnego nośnika energii w komórce. Pirogronian jest więc dosłownie bramą do wydajnej produkcji energii.
Gdy brakuje tlenu: Rola w fermentacji mlekowej
Sytuacja zmienia się diametralnie w warunkach beztlenowych (anaerobowych) lub przy niedostatku tlenu, na przykład w intensywnie pracujących mięśniach szkieletowych. Wtedy mitochondria nie mogą wydajnie przetwarzać pirogronianu. Aby glikoliza mogła zachodzić dalej i dostarczać chociaż minimalną ilość ATP, pirogronian musi zostać usunięty. W komórkach zwierzęcych ulega on redukcji do kwasu mlekowego (mleczanu) w procesie fermentacji mlekowej. Choć jest to proces mało wydajny energetycznie, pozwala na regenerację NAD⁺, niezbędnego do kontynuacji glikolizy, co w sytuacjach awaryjnych ratuje komórkę przed brakiem energii.
Centralna rola w metabolizmie to jednak nie jedyne oblicze kwasu pirogronowego.
Nie tylko biochemia – gdzie jeszcze spotkamy kwas pirogronowy?
Choć rola kwasu pirogronowego w metabolizmie jest absolutnie dominująca, związek ten występuje w przyrodzie również poza głównymi szlakami energetycznymi i znajduje ciekawe zastosowania praktyczne. Warto mieć świadomość tej szerszej perspektywy.
Naturalne źródła występowania w przyrodzie
Kwas pirogronowy nie jest związkiem syntetycznym, spotykamy go naturalnie w wielu produktach. Występuje on w niewielkich ilościach w niektórych owocach, na przykład w jabłkach. Co ciekawe, jego stężenie wzrasta w procesach fermentacji, dlatego można go znaleźć w sfermentowanych owocach czy niektórych produktach spożywczych poddawanych fermentacji. Jest to więc związek, z którym mamy kontakt w naszej codziennej diecie, choć zazwyczaj nie zdajemy sobie z tego sprawy.
Przeczytaj również: Skuteczne sposoby na pryszcze – jak się pozbyć niedoskonałości w 5 krokach
Zastosowanie w kosmetologii: Dlaczego jest składnikiem popularnych peelingów?
Jednym z najbardziej zaskakujących dla laika zastosowań kwasu pirogronowego jest kosmetologia i dermatologia estetyczna. Jest on popularnym składnikiem peelingów chemicznych. Ze względu na swoją strukturę α-ketokwasu i małą cząsteczkę, kwas pirogronowy łatwo penetruje w głąb skóry. Wykazuje tam silne działanie keratolityczne (złuszczające), pomagając usuwać martwe komórki naskórka. Ponadto działa seboregulująco, co jest cenne w terapii trądziku, oraz stymuluje produkcję kolagenu i elastyny w skórze właściwej, co daje efekt ujędrnienia i wygładzenia drobnych zmarszczek. To doskonały przykład na to, jak wiedza o budowie chemicznej związku pozwala znaleźć dla niego zupełnie nowe, praktyczne zastosowanie.